El Departamento de Agricultura de EE. UU. publicó esta semana una versión inédita de su análisis genético sobre el derrame y la propagación de la gripe aviar en el ganado lechero de EE. UU., ofreciendo la visión más completa hasta el momento de los datos que los investigadores estatales y federales han acumulado en el brote inesperado y preocupante. y lo que podría significar.
El análisis de la preimpresión proporciona varios conocimientos importantes sobre el brote: cuándo pudo haber comenzado realmente, cuánta transmisión nos estamos perdiendo, sorprendentes incógnitas sobre la única infección humana relacionada con el brote y cuánto continúa evolucionando el virus en las vacas. . La información es fundamental ya que los expertos en gripe temen que el brote esté aumentando el riesgo siempre presente de que este astuto virus de la gripe evolucione para propagarse entre los humanos y provocar una pandemia.
Pero no ha sido fácil conseguir la información. Desde el 25 de marzo, cuando el USDA confirmó por primera vez que un rebaño de vacas lecheras estadounidenses había contraído el virus de la influenza aviar H5N1, altamente patógeno, la agencia ha recibido críticas internacionales por no compartir datos de manera rápida o completa. El 21 de abril, la agencia vertió más de 200 secuencias genéticas en bases de datos públicas en medio de la presión de expertos externos. Sin embargo, muchas de esas secuencias carecen de metadatos descriptivos, que normalmente contienen información básica y clave, como cuándo y dónde se tomó la muestra viral. Los expertos externos no tienen esa información crucial, lo que hace que los análisis independientes sean frustrantemente limitados. Por lo tanto, el nuevo análisis del USDA, que presumiblemente incluye esos datos, ofrece la mejor visión hasta ahora de la información completa sobre el brote.
Propagación no detectada
Una de las principales conclusiones es que los investigadores del USDA creen que la propagación de la gripe aviar de las aves silvestres al ganado comenzó a finales del año pasado, probablemente en diciembre. Por lo tanto, el virus probablemente circuló sin ser detectado en las vacas lecheras durante unos cuatro meses antes de que el USDA confirmara el 25 de marzo una infección en un rebaño de Texas.
Esta conclusión sobre el cronograma se alinea en gran medida con lo que expertos externos previamente recopilados de los limitados datos disponibles públicamente. Por lo tanto, puede que no sorprenda a quienes siguen el brote, pero es preocupante. Meses de propagación no detectada plantean importantes preocupaciones sobre la capacidad del país para identificar y responder rápidamente a los brotes de enfermedades infecciosas emergentes, y si las respuestas de salud pública han superado los errores observados en las primeras etapas de la pandemia de COVID-19.
Pero otro gran hallazgo de la preimpresión es cuántas lagunas todavía existen en nuestra comprensión actual del brote. Hasta la fecha, el USDA ha identificado 36 rebaños en nueve estados que han sido infectados con H5N1. La buena noticia del análisis genético es que el USDA puede trazar líneas que conectan la mayoría de ellos. Los investigadores del USDA informaron que el «movimiento directo de ganado basado en prácticas de producción» parece explicar cómo el H5N1 saltó de la región del Panhandle de Texas (donde se cree que ocurrió el contagio inicial) a otros nueve estados, algunos tan remotos como Carolina del Norte. Michigan e Idaho.
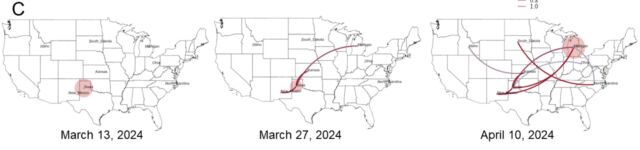
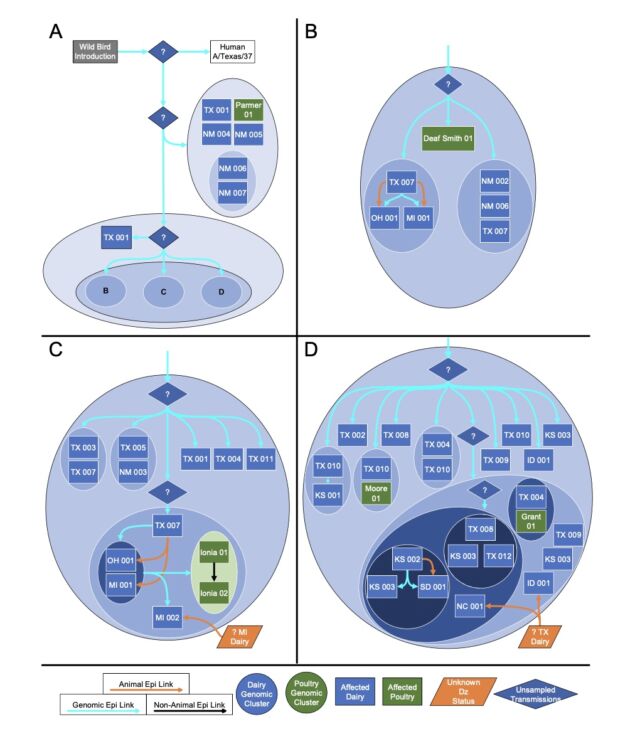
Vías de transmisión putativas del genotipo B3.13 del clado 2.3.4.4b de HPAI H5N1 respaldadas por vínculos epidemiológicos, movimientos de animales y análisis genómicos. [/ars_img]La mala noticia es que esas líneas que conectan los rebaños no son sólidas. Hay lagunas en las que los datos genéticos sugieren que se produjo una transmisión no identificada, tal vez en vacas no muestreadas, tal vez en otros animales por completo. Los datos genéticos son claros: una vez que esta cepa de gripe aviar (H5N1 clado 2.3.4.4 genotipo B3.13) saltó al ganado, podría propagarse fácilmente a otros mamíferos. Los datos genéticos vinculan los virus del ganado que se trasladan muchas veces a otros animales: hubo cinco saltos de ganado a aves de corral, una transmisión de ganado a mapaches, dos eventos en los que el virus pasó del ganado a los gatos domésticos y tres veces en las que el virus pasó. del ganado repercutió en las aves silvestres.
«No podemos excluir la posibilidad de que este genotipo esté circulando en lugares y huéspedes no muestreados, ya que el análisis existente sugiere que faltan datos y la falta de vigilancia puede oscurecer la transmisión inferida utilizando métodos filogenéticos», escribieron los investigadores del USDA en su preimpresión.
